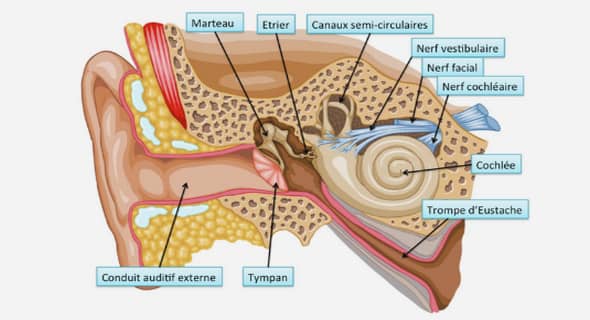
Les méthodes d’étude de résistance
Méthodes
Pour faire ce travail, nous avons adopté la méthodologie suivante : Pour l’étude de la chimiosensibilité des parasites aux antipaludiques, nous avons utilisé le test SYBR Green ex vivo. Pour le polymorphisme génétique de Pfcrt et Pfmdr1, nous avons utilisé la HRM.
Test ex vivo
Principe
Le test consiste à mettre en culture un isolat de Plasmodium falciparum pendant 48 à 72h en présence de molécule antipaludique et de faire la quantification de l’ADN parasitaire en utilisant la molécule SYBR Green. La molécule SYBR Green se fixe spécifiquement sur l’ADN du parasite et émet une fluorescence bleue (max 535 nm) lorsqu’il est éclairé avec une lumière ultraviolette (max485 nm). Cette propriété du SYBR Green a été mise à profit pour évaluer la sensibilité des molécules. Le SYBR Green ou le C32H37N45 est une molécule fluorescente qui permet de détecter et de quantifier l’ADN grâce à un appareil appelé PLATE READER ou FLUORESKAN (Figure 8). Une technique semblable a été utilisée pour étudier la sensibilité d’isolats de P. falciparum à différentes molécules antipaludiques par (Ndiaye et al., 2010) dans le cadre d’une étude ex vivo avec la molécule de DAPI. Figure 8: Longueurs d’onde d’excitation de : (1) SYBR Green I, (2) tous rapports de complexes SYBR green I/ADN double brin, (3 et 4) complexe SYBR green I/ADN simple .
Mode opératoire
Le test ex vivo peut être subdivisé en quatre étapes : – La préparation des plaques de culture, contenant les molécules à tester. – La culture proprement dite. – La quantification de l’ADN parasitaire – La détermination ou le calcul de la Cl50 en utilisant le logiciel Graph pad Prism.
Préparation des solutions et des plaques de culture
Cette préparation, se fait généralement avant la période de collecte et nécessite des plaques de 96 puits, du solvant DMSO (diméthylsulfoxyde), des molécules antipaludiques (disponibles en poudre), du milieu Roosvelt Park Memorial Institute (RPMI) et de l’eau distillée. Elle consiste à préparer les solutions d’antipaludiques et à les distribuer dans des plaques de culture de 96 puits. Les antipaludiques étant sous forme de poudre, ils sont d’abord dissouts dans un solvant (DMSO, Eau ou Méthanol). Les solutions filles sont ensuite distribuées dans les plaques en respectant une série de dilution au demi. Sur la tableau 5 nous avons plaque de culture avec les concentrations initiales diluées de quelques molécules (voir série de dilution en annexe)
Culture
Les tubes de sang veineux sont reçus au laboratoire de biologie moléculaire de l’hôpital Aristide Le Dantec. Une fois au laboratoire le sang est transféré dans un tube Falcon de 15 ml puis centrifugé (2500g pendant 10 min) pour séparer le plasma et le culot globulaire. Le culot est lavé deux fois de suite avec du RPMI incomplet par centrifugation à 2500g pendant 5 min pour éliminer les composantes de l’immunité (anticorps et leucocytes). Pour que l’échantillon soit cultivé la parasitémie doit être comprise entre 0,4 et 1% et l’hématocrite a été ajusté à 2%. Pour cela, 24,5 mL de milieu RPMI complet est mélangé avec 0,5 mL de sang parasité. Le mélange ainsi obtenu est distribué dans les plaques de cultures (préchargées de 10 µL d’antipaludique) à raison de 90µL par puits. Les plaques sont placées dans une enceinte hermétique en présence d’un mélange de gaz (94% N2, 5% de CO2, 1% d’O2) et incubées à 37 ° C (Figure 9). Après 48 h d’incubation, un premier contrôle de la croissance parasitaire est effectué sur les lames de contrôles. Les plaques sont congelées à 20°C jusqu’à la lecture.
Lecture des plaques
Pour la lecture des plaques nous préparons une solution SYBR Green-Tampon. Pour cela, un mélange a été préparé à l’avance et conservé à la température ambiante. 0,2 µl de la solution SYBR Green (SYBR Green I acide nucléique gel Stain 10 000 ×, Sigma Aldrich) était mélangée avec 1 ml de la solution Tampon (solution de lyse). Le tampon de lyse contenait du Tris (20 mM, pH 7,5), de l’EDTA (5 mM), saponine (0,008% poids / volume) et Triton X-100 (0,08% volume / vol) (Rason et al., 2008). Un mélange 100 µl de la solution SYBR Green-Tampon a été distribué dans chaque puits. Après mélange, une incubation d’une heure est effectuée. La quantification de l’ADN parasitaire est ensuite faite de façon indirecte en mesurant la fluorescence émise dans chaque puits à l’aide du Fluoroskant Ascent (Tableau 6).
Détermination des CI50
Les valeurs de CI50 ont été calculées à l’aide du logiciel graphique Pad Prism version 5. Le Clone de référence 3D7, sensible à tous les médicaments antipaludéens testés, a été utilisé pour chaque lot de plaques comme un contrôle technique.