Fusarium oxysporum f. sp. albedinis
Historique et Taxonomie
Le genre Fusarium
Le genre Fusarium a été décrit par Link en 1809 (Booth, 1985), et sa délimitation actuelle a été faite par Appel et Wollenweber en 1910, et depuis cette année, de nombreux travaux ont été consacrés pour sa taxonomie (Wollenweber et Reinking, 1935 ; Snyder et Hansen, 1940 ; Raillo, 1950 ; Gordon, 1952 ; Messiaen et Cassini, 1968 ; Booth, 1971 ; Joffe, 1974 ; Nelson et al., 1983).
Le nom du genre Fusarium est tiré du latin « fusus », vu qu’il a des spores en forme de fuseau. Il comporte 9 espèces phytopathogènes.
L’espèce Fusarium oxysporum
Wollenweber et Rincking (1935) ont placé l’espèce oxysporum dans la section « Elegans » , qu’ils ont subdivisé en 03 sous-sections, en se basant sur la forme et la taille des spores et sur les caractères culturaux (Ghomari, 2009).
Dès 1940, toutes les espèces de la section « Elegans » sont rassemblées dans une seule espèce Fusarium oxysporum, par Synder et Hansen, à laquelle, Synder et al., adjoignent le cultivar « redolens » en 1957 (Ghomari, 2009).
Dans le genre Fusarium, l’espèce oxysporum, constitue 50% à 70% des populations « fusariennes » des sols (Guillemat et Montegut, 1958; Gorden1965 ; Mc Mullen et Stack, 1983). Elle est considérée comme colonisatrice primaire du rhizoplan et du cortex racinaire. Elle représente plus de 50 % des isolats de Fusarium à partir des racines de plantes diverses (Bruel, 1976 ; Mc Mullen et Stack, 1983).
L’espèce oxysporum, peut vivre en saprophyte ou en parasites de vertébrés ou de plantes (Nelson et al., 1981 ; Rebell, 1981, in Bounaga, 1991). Sa forme parfaite n’est pas encore connue. L’espèce Fusarium oxysporum se distingue des autres espèces de Fusarium par la production abondante de microconidies, rassemblées en fausse tête qui repose sur des monophialides courtes (Burgess et Lidell, 1983). Seule la reproduction asexuée a été observée chez cette espèce, ce qui la place dans le groupe des Deuteromycetes (champignons imparfaits, Fungi imperfecti).
Des formes sexuées (téléomorphes) ont été maintenant observées pour certaines espèces de Fusarium. Elles font toutes partie des Ascomycètes, de la famille des Nectriales et notamment des genres Gibberella et Nectria (Seifert, 2001) .
Ainsi, Fusarium oxysporum est considéré comme ascomycète bien que le stade sexuel doive être encore trouvé. Il est proposé d’être plutôt proche du groupe téléomorphique Gibberella que Nectria (Di Pietro et al., 2003, Michielse et Rep, 2009).
La forme spéciale Fusarium oxysporum f. sp. albedinis
Il y a plus de 120 formae speciales décrites chez Fusarium oxysporum, chacune inféodée à une plante hôte particulière (Di Pietro et al., 2003). La reconnaissance de ces formes spéciales, ne fait appel à aucun critère morphologique mais seulement à la pathogénicité du champignon, dont la détermination doit se faire par la réinoculation du pathogène dans la plante hôte (Bounaga, 1991).Parmi ces formes spéciales, on distingue « albedinis », qui responsable de la fusariose vasculaire du Palmier dattier connue par le « Bayoud » (Bounaga, 1991).
Position systématique
La nouvelle classification taxonomique basée sur la phylogénie moléculaire selon (Debourgogne, 2013) est la suivante :
Règne……………………… Fungi
Division…………………… Ascomycota
Classe……………………… Sordariomycetes
Sous-classe………………… Hypocreomycetidae
Ordre………………………. Hypocreales
Famille……………………… Nectriaceae
Genre……………………….. Fusarium
Caractères physiologiques du champignon
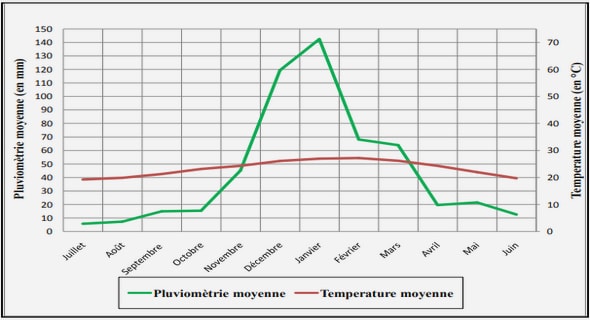
Le milieu favorable au développement de Fusarium est à base de pomme de terre (PDA) (Bouhot et Billotte, 1964). Sa croissance minimale est entre 7°C et 12°C, elle devient optimale entre 21°C et 27,5°C, et elle s’arrête à 37°C (Malençon, 1947). La croissance de ce champignon est faible entre les pH 8,5 et 9,7 et rapide entre les pH 5 et 6. Ainsi, les sources de carbone les mieux métabolisées sont : la pectine, le mannose et le glucose. Les sources d’azote organique sont mieux assimilées par ce champignon que l’azote minéral (Arib, 1998).
Description morphologique
Le Fusarium oxysporum f. sp. albedinis est un champignon avec un mycélium aérien qui a une pigmentation variable (Blanchâtre, rosâtre, violette, mauve, orange ou beige) qui est due à la formation d’une multitude de spores en surface par des orages fructifères (sporodochies, pionnotes), ainsi qu’aux variations de la lumière et du milieu de culture (Messaoudi et al., 1989).
Ce champignon possède un mycélium cloisonné, fin et régulier en culture jeune. Ce mycélium présente des cellules hypertrophiées en chaine, d’aspect globuleux en cultures âgées ayant une grande ressemblance avec les chlamydospores, mais sans épaississement de la paroi (Ghomari, 2009). Ce champignon est caractérisé par la production de :
• Microconidies : sont très nombreuses, hyalines de forme et de dimension variables dans une même culture (3-15 x 3-5 µm). Les microconidies sont souvent unicellulaires, parfois bicellulaires et possèdent une cloison.
• Macroconidies : sont peu nombreuses, fusiforme, avec une extrémité pointue et courte. Elles possèdent trois cloisons, rarement 4 ou 5 et mesurent (20-35 x 3-5 µm).
• Chlamydospores : dans les cultures âgées ou dans le sol, le Fusarium oxysporum f.sp. albedinis forme des chlamydospores, régulières, soit globuleuses, à paroi lisse et épaisse, et leur taille varie de 6 à 20 µm. Elles sont intercalaires ou terminales et sont isolées ou groupées par (Bulletin OEPP, 2003).
Plantes hôtes
La plante hôte principale est le palmier dattier. Tous les cultivars nord-africains de qualité sont sensibles (Mejhoul, Deglet Nour, Bou Feggous, etc.). Certains cultivars ont une bonne résistance (Bou Sthammi noir, Bou Sthammi blanc, Tadment, Iklane, Sair Laylet, Bou Feggous ou Moussa au Maroc et Takerboucht en Algérie), mais parmi ces cultivars, seuls Sair Laylet et Takerboucht sont de qualité acceptable, quand même inférieure à celle de Deglet Nour ou Mejhoul (Djerbi, 1983 ; IMI, 1994) .
On signale aussi Fusarium oxysporum f. sp. albedinis sur d’autres plantes cultivées dans les palmeraies: le henné (Lawsonia inermis L.) une plante tinctoriale; la luzerne (Medicago sativa L.) et le trèfle (Trifolium sp.). Ces plantes sont considérées comme des « porteurs sains », elles peuvent héberger l’agent causal du bayoud sans manifester le moindre symptôme externe, mais montrent au contraire des nécroses internes au niveau des racines et du collet (Arib, 1998), et sont largement cultivées en Afrique du Nord et au Proche-Orient (Djerbi, 1983 ; IMI, 1994).
INTRODUCTION |