La chromatographie Supercritique (SFC)
Bien que l’emploi d’un fluide supercritique pour réaliser une analyse chromatographique ne soit pas une technique récente (première publication datant de 1962 [49]), plusieurs évolutions des appareillages ont redonné un véritable intérêt pour l’utilisation de la SFC. Cette dernière utilise des colonnes de séparation de type colonne remplies et un gradient de co-solvant associé au CO2 pour l’élution des composés. Pour ce type de SFC, l’ajout d’un régulateur actif de pression en sortie de colonne, le développement de pompes calorifugées et la maîtrise totale de l’introduction de l’échantillon dans le circuit sous pression ont permis d’augmenter la robustesse et la fiabilité des analyses. Désormais, il est possible d’exploiter au maximum les propriétés de ces phases mobiles spécifiques et de coupler ceci au large éventail de phases stationnaires utilisées en LC. L’élution d’une grande gamme de composés est possible sans risquer de les dégrader thermiquement. Bien comprendre les spécificités des phases mobiles et stationnaires employées en SFC afin de cerner au mieux l’intérêt d’une telle technique pour la caractérisation des huiles de pyrolyse rapide est donc nécessaire. Après plusieurs essais employant une large variété de fluides, le choix du dioxyde de carbone (CO2) est apparu comme unanime. En effet, ce dernier regroupe plusieurs avantages : fluide peu coûteux, non inflammable, facilement disponible en qualité supérieure, inerte et présentant une faible absorbance en UV. A cela s’ajoute des conditions critiques facilement maintenues (71 bars et 31 °C) et surtout un large panel de solvants organiques miscibles (261 substances recensées par A.W. Francis [49]).
Cependant, le CO2 seul reste limité pour la solubilisation de tous les analytes. C’est pourquoi actuellement, la grande majorité des analyses SFC emploient une phase mobile composée de CO2 et d’un co-solvant organique pour augmenter cette solubilité et éviter des phénomènes de précipitation lors de l’injection des échantillons. L’augmentation du taux de co-solvant va donc induire une modification du pouvoir solvant de la phase mobile au cours du temps. D’autre part, ces co-solvants vont aussi permettre de réduire l’élargissement des pics en réduisant les interactions non désirées avec les phases stationnaires. Typiquement, la phase mobile d’une méthode SFC pour l’analyse d’un échantillon constitué de composés de polarité très variable correspondra à un mélange de CO2 et de co-solvant pouvant varier entre 5 et 50 % au cours de l’analyse [51]. En modifiant ainsi la composition de la phase mobile, on modifie également les valeurs critiques de cette phase mobile. La Figure I-15 montre comment évoluent ces valeurs lorsqu’on augmente la quantité de co-solvant, dans ce cas le méthanol.
Plus le taux de co-solvant augmente et plus la température critique augmente. La pression critique quant à elle, va passer par un maximum avec l’augmentation de co-solvant (par exemple pour le MeOH aux alentours de 40%) avant de diminuer de nouveau [52]. Bien que le CO2 permette l’utilisation de différents co-solvants, la majorité des travaux publiés emploient un alcool (méthanol, éthanol et isopropanol) (Cf. Figure I-16) offrant la possibilité d’interagir avec les groupes silanols de la phase stationnaire et de réduire ainsi l’élargissement de pics dû à ces derniers [54,55]. Le caractère non polaire du CO2 a souvent conduit les utilisateurs à employer des phases stationnaires polaires, ce qui pouvait s’approcher de la chromatographie en phase liquide à polarité de phase normale. Cependant, l’ajout d’un co-solvant organique dans la phase mobile permet également l’utilisation de colonnes habituellement employées en chromatographie en phase liquide à polarité de phase inversée. Ces différentes possibilités ont été investiguées dans divers travaux de la littérature [56,57]. L’ajout de co-solvant dans le CO2 compressé permet donc l’unification des deux domaines distincts en chromatographie liquide offrant ainsi une large gamme d’applications possibles (Tableau I-3).
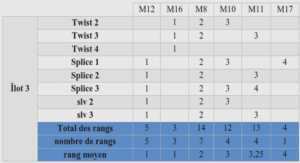
Ce large choix représente aussi une difficulté lors de l’élaboration d’une méthode. Il est en effet impossible de tester toutes les phases stationnaires disponibles sur le marché. Les travaux de West et al., basés sur les descripteurs d’Abraham [58,59] et le modèle LSER (Linear Solvation Energy Relationship) (Eq.1) ont permis de classifier les différentes chimies de phase stationnaire en fonction des interactions mises en jeu. Cette équation permet de relier la rétention d’un composé donné (log k) à différents paramètres physico chimiques de ce composé (correspondant aux termes en majuscule) dans un certain système de phase stationnaire, phase mobile, température et BPR, caractérisé lui-même par des descripteurs (indiqués en minuscule). En employant une régression multilinéaire basée sur les descripteurs connus de certaines molécules, il est alors possible de déterminer les termes liés au système. Au travers de plusieurs séries d’expérimentations, un comparatif a pu être mis en place entre la plupart des phases stationnaires disponibles actuellement sur le marché : alkyls [61], aromatiques [62–64] et polaires [65].