Enjeux sociétaux, économiques et environnementaux
Document destiné aux enseignants pour élaborer les séquences d’enseignement (cours / TD) relatives à la chimie verte (les fondements, les agroressources, les notions d’économie atomique et de facteurs environnementaux), à l’utilisation des solvants et à leur remplacement ou leur limitation (solvants supercritiques, liquides ioniques, transfert de phase, réactifs supportés), aux réactifs et procédés « verts » (micro-ondes, ultrasons). Des activités expérimentales sont indiquées ou suggérées. Relativement simples à réaliser, elles permettent d’utiliser d’emblée les méthodes modernes de synthèse qui seront mises en œuvre, autant que possible, dans les autres parties du programme. Il semble souhaitable de traiter cette partie en début d’année, comme cela est suggéré par la place occupée dans le référentiel. Cela permet de poser les notions de base et de bien présenter l’esprit du nouveau programme en accord avec les préoccupations actuelles de la chimie. Des notions de nomenclature sont utiles mais elles peuvent être introduites au fur et à mesure des besoins, surtout pour montrer la logique de la construction des noms. La partie « efficacité atomique » nécessite de savoir équilibrer une réaction chimique.chimie verte, agroressources, économie d’atomes, facteur environnemental, solvant, solvant supercritique, liquide ionique, catalyse par transfert de phase, ammoniums quaternaires, éthers couronnes, cryptands, réactifs supportés, argiles, silice, alumine, résines échangeuses d’ions, réactions sans solvants, micro-ondes, ultrasons, sonochimie.
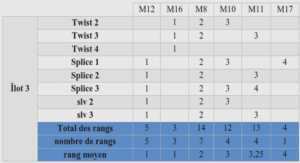
On voit que le facteur E augmente beaucoup avec la complexité des produits fabriqués (plus d’étapes de synthèse) et que finalement la quantité de déchets produits par l’industrie pharmaceutique est comparable à celle produite par la chimie lourde alors que la masse de produit commercialisé est de 100 à 1000 fois plus faible !Il est bien sûr possible de réaliser ces manipulations – l’oxydation des alcools est prévue – et d’utiliser les résultats. Si ces synthèses sont réalisées plus tard, il est intéressant de faire calculer les différentes grandeurs définies ci-dessus et de les commenter, dans le cadre de l’exploitation du TP (remarque valable pour toutes les synthèses effectuées).C’est le principe actif de nombreux produits « anti-douleurs » en vente libre. Il a été découvert par la société Boots (GB) en 1961. Elle le commercialise en 1964 et en fait breveter la synthèse (U.S. Patent 3,385,886). Elle détient alors le monopole de la fabrication jusqu’à Mai 1985. Avec d’autres firmes (sous licence Boots) elle a également le monopole de la vente jusqu’à Septembre 1986. Cette méthode en six étapes, la seule utilisée pendant la durée de validité du brevet, produit 1,5 fois plus de sous-produits que d’ibuprofène ! La production annuelle d’ibuprofène étant de l’ordre de 13000 tonnes, c’est plus de 20000 tonnes de sous-produits qui sont générés.
Ils sont soit retraités soit détruits. Ce sont des solutions diluées d’acide acétique et d’acide chlorhydrique, peu chers donc peu intéressants à recycler, donc traitement et destruction. Après l’expiration des droits plusieurs synthèses plus efficaces sont mises au point et plusieurs médicaments sont mis sur le marché. Le consortium BHC (Boots Company-Hoechst Celanese, racheté ensuite par BASF) est créé le 21 Avril 1988, aux USA, pour commercialiser l’ibuprofène. En 1991 BHC met au point et fait breveter un procédé en trois étapes (U.S. Patents 4,981,995 et 5,068,448). Cette nouvelle synthèse est beaucoup plus efficace. Le seul sous-produit, l’acide acétique, est récupéré et commercialisé. De plus les différents catalyseurs sont recyclés efficacement (acide fluorhydrique, nickel de Raney et palladium).Que ce soit un solvant de réaction ou d’extraction, il doit être finalement séparé des composés solubilisés. Ceci se fait, soit par modification de son pouvoir solubilisant (refroidissement, addition d’un moins bon solvant, puis filtration), soit par évaporation. Il faut donc qu’il ait une température d’ébullition aussi basse que possible, car dans la majorité des cas il finira par être distillé : lors de la séparation et lors de sa purification pour recyclage. * D’un autre côté, certaines réactions, plus difficiles, nécessitent de choisir un solvant de même catégorie mais avec une plus haute température d’ébullition (remplacement de l’éther par le THF (oxolane) ou le 1,4-dioxane pour la synthèse de certains organomagnésiens). Mais cela peut en partie être évité avec des méthodes d’activation non thermiques : micro-ondes, sonochimie.
Les liquides ioniques sont de plus en plus utilisés en tant que solvant et/ou de catalyseur (les anions AlCl4- ou Al2Cl7- remplacent AlCl3 en tant qu’acide de Lewis) dans les alkylations et les acylations de Friedel-Crafts. Ils permettent d’améliorer les rendements, la sélectivité et les vitesses de réaction. Étant donné leur faible volatilité, les températures de réaction peuvent être plus élevées, d’où des temps de réaction beaucoup plus courts ; le chauffage peut aussi être effectué par micro-ondes. L’extraction est facilitée (ajout d’un support solide, flash chromatographie…), l’acide de Lewis est recyclé car faisant partie du liquide ionique. Les conditions n’ont pas besoin d’être strictement anhydres (pas d’atmosphère anhydre). Par exemple l’acétylation du naphtalène par le chlorure d’acétyle se déroule en 5 min à 0°C dans le tétrachloroaluminate de 1-éthyl-3-méthylimidazolium (EtMeA1-Cl + 67% AlCl3) et donne la meilleure sélectivité connue pour l’acylation en position 1 par rapport à la position 2 : rapport de 45 à 1 au lieu de 5 à 1 dans les conditions classiques.