Diagnostic biologique des hémoglobinopathies chez les nourrissons
Rappel sur l’hémoglobine
Structure de l’hémoglobine
L’hémoglobine est une chromoprotéine constitué d’une partie protéique ( la globine), et d’une partie non protéique (l’hème). Les hémoglobines possèdent quatre protomères (sous -unités) identiques deux à deux. Les sous-unités sont constituées de l’association d’une chaîne polypeptidique, la globine, et d’un groupement prosthétique, l’hème. Les différences entre hémoglobines portent sur la séquence des chaînes peptidiques, alors que l’hème est identique dans toutes les cellules (Crossley et Orkin, 1993). Il existe chez l’homme quatre variétés physiologiques d’hémoglobines et de nombreuses formes pathologiques n’ayant pas toutes d’expression clinique. On trouve chez l’adulte un type prédominant, l’hémoglobine A ou A0 (97 à 98%), un type mineur, l’hémoglobine A2, représentant 2 à 3 % de l’hémoglobine totale et l’hémoglobine feotale est appelée hémoglobine F. Toutes les hémoglobines renferment 0.34% de fer impliquant une masse moléculaire de 16500 daltons par atome de fer. La masse moléculaire de l’hémoglobine est d’environ 67000 daltons(Figure1) (Vanbourdolleet al, 2007). Figure 1. Schéma de la molécule complète d’hémoglobine. • Tétramère :(2 α /2 β). • Un hème. • Un atome de fer ferreux.
L’hème
L’ensemble « fer incorporé à une porphyrine » constitue un hème. Dans le cas de l’hémoglobine, la porphyrine abritant l’atome de fer est la protoporphyrine, molécule hautement conjuguée, plane et donneuse d’électrons .L’hème est coordonné à l’histidine proximale de la chaîne protéique globine et à l’oxygène (De Franceschi et Corroche, 2004) (Figure 2). Figure 2. Structure de l’hème.
La globine
C’est un ensemble de quatre chaînes polypeptidiques avec pour chaque molécule de l’Hb quatre chaînes semblables deux à deux sont appelées α et β pour l’HbA. (Globine de l’HbA = 2α/2β) (Hargrove et al, 1997). Chaque chaîne est un polypeptide c’est-à-dire qu’elle est constituée d’acide aminé (146 pour la chaîne β et 141 pour la chaîne α) réunis par des liaisons peptidiques. La chaîne ainsi formée s’enroule sur elle-même en spiral pour réaliser une structure secondaire en hélice. En fait, l’hélice est discontinue, l’ensemble de la chaîne formant 8 segments hélicoïdaux (A à H) et porte une crevasse entre hélices E et F où s’insère une molécule d’hème. (Rivière et Sadelain, 1997). 6 Ces segments sont séparés par de courts segments non hélicoïdaux au niveau des quels se font des coudures pour donner à chaque chaîne sa forme définitive. Des liaisons de nature diverses entre acides aminés mise en évidence en contacte par les courbures de la molécule la stabilisent (structure tertiaire). Enfin la réunion de 2 chaînes α et de 2 chaînes β forme une molécule symétrique globulaire (Bernard et al, 1998). La forme désoxygénée de l’hémoglobine présente une conformation T (tendue), la forme oxygénée une conformation R (relaxée) (Bachir et Beauvais, 1992). L’architecture de cette protéine globulaire compacte avec des dépressions, interfaces entre domaines et crevasses lui permet d’assurer ces fonctions dynamiques (Figure3). Figure 3. Modification de la conformation de l’hémoglobine après oxygénation.
Répartition des hémoglobines normales de l’homme
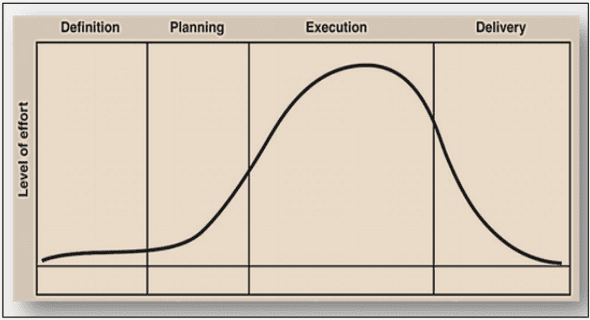
Différentes hémoglobines (Hb) se trouvent successivement mises en évidence au cours du développement humain. Pendant la période embryonnaire, différents types de chaînes vont être synthétisés (figure 4), δ , ε, puis, progressivement, α et γ. Dès le 37e jour de vie fœtale, apparaît l’hémoglobine fœtale, Hb F ou α2γ2, formée de l’association de deux chaînes α et de deux chaînes γ. L’Hb F, dont environ 15 % est sous forme acétylée, reste l’hémoglobine majoritaire tout au long de la vie fœtale jusqu’à la naissance. Le remplacement des chaînes γ par des chaînes β se fait progressivement jusqu’à l’âge d’un an chez le sujet normal, pour donner l’hémoglobine adulte, 2α/2 β (Hb A). Ainsi, à 30 semaines de vie fœtale, seulement 10 % de l’hémoglobine est de l’Hb A, contre environ 25 % à la naissance pour un bébé né à terme, et 75 % vers l’âge de trois mois. 7 Après l’âge d’un an, l’hémoglobine est constituée d’environ 97 % d’Hb A et de 2 à 3% d’Hb A2 (α2δ 2). Le taux d’Hb F est souvent inférieur à 1 % vers l’âge d’un an, mais il peut décroître plus tardivement. Figure 4. Biosynthèse des chaînes de globine au cours de la vie fœtale et jusqu’à l’âge de 6 mois. (Rosa et al, 1993).
Fonction de l’hémoglobine
L’hémoglobine assure le transport de l’oxygène des poumons vers les tissus. Une molécule d’oxygène se fixe par atome de fer et 1 g d’hémoglobine peut transporter au maximum 1,34 ml d’oxygène lorsque la saturation est totale, soit environ 20ml d’oxygène pour 100 ml de sang. (Figure 5) La courbe de saturation de l’hémoglobine en fonction de la pO2 présente une allure sigmoïde d’un point de vue moléculaire, cette fixation est un phénomène coopératif (en relation avec l’allostérie) dû à l’association et au recrutement différent des quatre sous-unités de l’hémoglobine. Le segment initial de la courbe correspond à l’oxygénation du premier sousunité du tétramère et témoigne d’une faible affinité de celle-ci pour l’oxygène. 8 Figure 5. Courbe de saturation de l’hémoglobine. (Arthur et Guyton,1974). La pente de la courbe traduite la coopérativité. Le segment terminal de la courbe correspond quant à lui à l’oxygénation de la dernière sous-unité et révèle sa forte affinité pour le ligand. L’oxygène se comporte comme un ligand qui stimule le changement de conformation de chaque sous-unité. La fixation d’une première molécule est relativement lente. L’oxygénation de cette première sous-unité entraîne la fixation d’oxygène successivement sur les autres sous-unités d’une façon auto catalytique. (Faivre-Fiorina et al, 1998). Pour une pO2 100mmHg, correspondant à la pression de l’alvéole pulmonaire. L’hémoglobine est saturée complètement (97,5%). En revanche, au niveau des tissus où la pO2 est de 35 mmHg. La combinaison de l’hémoglobine à l’oxygène s’exprime en termes de pourcentage (%) de saturation, soit le rapport de l’oxyhémoglobine à l’hémoglobine totale. L’équilibre Hb + O2 (HbO2) est réglé par la pO2. L’oxygène sanguin est combiné pour 98,5% de sa totalité. La faible part restante joue un rôle capital et assure la pO2 l’oxyhémoglobine libère l’oxygène au fur et à mesure que la pO2 diminue. Plusieurs autres facteurs influencent l’affinité de l’hémoglobine pour l’oxygène, le principal étant la pression partielle en oxygène (plus la pression en oxygène est élevée et plus l’affinité de l’Hb pour l’oxygène baisse), mais également divers autres : baisse du pH, augmentation de la température ou augmentation du 2,3 DPG auront pour effet une baisse de l’affinité de l’hémoglobine pour l’oxygène. (Vanbourdolleet al, 2007). I.4. Biosynthèse et catabolisme de l’hémoglobine
La biosynthèse
La biosynthèse de l’hémoglobine est réalisée chez l’adulte dans les érythroblastes de la moelle osseuse et dans les réticulocytes circulants. 9 Les précurseurs de l’hémoglobine sont : – les chaînes polypeptidiques de la globine ; – la protoporphyrine, synthétisée dans les mitochondries cellulaires des tissus ; – Le fer provenant essentiellement du recyclage interne. L’insertion de fer ferreux au centre de la protoporphyrine forme l’hème.
Synthèse des chaînes polypeptidiques de la globine et contrôle génétique
Comme toute protéine, la globine est synthétisée par : – transcription : copie, sous forme d’une structure de base complémentaires, d’une partie d’ADN correspondant à un gène de structure et formation d’un ARNm d’abord natif puis fonctionnel par perte des régions non codantes ; – Traduction : elle permet de traduire une séquence de nucléotides en séquences d’acides aminés et comprend trois étapes (initiation, élongation puis libération des chaînes polypeptidiques). – activation des acides aminés : par fixation des acides aminés cytoplasmiques sur un ARNt spécifique. Chez l’homme, les gènes de l’hémoglobine se répartissent en deux groupes distincts: – le groupe des gènes de type α ; – le groupe de gène de type β La structure de tous les gènes de globine est similaire : chacun est formé de deux introns (région non codantes) et de trois exons (régions codantes). La région transcrite est précédée d’un promoteur (boites TATAA et CCAAT) et de séquences régulatrices en amont qui synchronisent l’expression des gènes des différentes globines en fonction des cellules érythropoïétines. Toutes les hémoglobines humaines sont des tétramères associant deux sous-unités du type α et deux autres du type β. Physiologiquement, il y a toujours un équilibre de synthèse entre les chaînes-α et -β de globine. (Sébahoun G, 2005).
Groupe des gènes de type α
Il est localisé sur le chromosome 16, Il comprend de 3´ à 5´ (sur une petite séquence de ADN de 35Kb): – deux gènes de structure α1 et α2, fonctionnels dès la vie embryonnaire ; 10 – un gène de structure δ permettant la formation des chaînes δ (qui remplacent les chaînes α au cours des premiers semaines de la vie embryonnaire). Chez un sujet normal, les gènes α1 et α2 sont dupliqués. Il existe donc quatre gènes de structure α pour une paire de chromosomes. En revanche, les gènes α2 sont trois fois plus exprimés que les gènes α1 (figure 6) (Sadelain, 2006).
Groupe des gènes de type β
Il est localisé sur le bras court du chromosome 11(dans un fragment d’ADN de 60 Kb) et il comprend de 5´ vers 3´ : – un gène β, dont l’expression débute à la fin du premier trimestre de gestation ; – un gène δ, fonctionnel après la naissance ; – deux gènes γA et γG qui diffèrent par la variation d’un acide aminé en position 136 de la chaîne fœtale (glycine et alanine) ; – un gène ε embryonnaire. Le gène β n’est pas dupliqué, contrairement aux gènes α. Les lésions qui touchent les gènes β s’expriment : – pour 50% de l’hémoglobine totale si un seul gène est atteint ;- pour 100% de l’hémoglobine totale si aucun des deux gènes n’est fonctionnel .
INTRODUCTION |