Caractéristiques des NMOSD
Une méta-analyse étudiant l’épidémiologie de la NMO dans le monde, selon les critères de Wingerchuk de 2006, retrouvait des incidences variables entre les pays, allant de 0.053/100000 personnes par an à Cuba à 0.4/100000 personnes par an dans le sud du Danemark. La prévalence allait de 0.51/100000 à Cuba à 4.4/100000 dans le sud du Danemark. On remarquait une prédominance féminine et un âge moyen de début allant de 30 ans pour l’Iran à 39.5 ans pour le sud du pays de Galles7. Il existerait une prédilection pour les non-caucasiens, même si toutes les populations semblent touchées8. Bien que les cas de NMOSD soient habituellement sporadiques quelques formes familiales ont été rapportées9. Névrite optique (nécessite une IRM encéphalique ne montrant pas d’atteinte ou des anomalies non spécifiques de la substance blanche, ainsi qu’une atteinte de plus de la moitié du nerf optique ou du chiasma optique (Hypersignal T2 ou prise de contraste de gadolinium en T1)). hétérogénéité au sein des NMOSD. Il convient de noter que parmi les NMOSD AQP4- IgG séronégatives, certains présentent des anticorps anti-Myelin Oligodendrocyte Glycoprotein (MOG) ayant des caractéristiques différentes de celles retrouvées chez les NMOSD avec anticorps anti-AQP4 (les hommes sont plus touchés, les poussées sont moins fréquentes et concernent habituellement les nerfs optiques et la partie caudale de la moëlle épinière, la récupération de ces dernières serait par ailleurs meilleure).
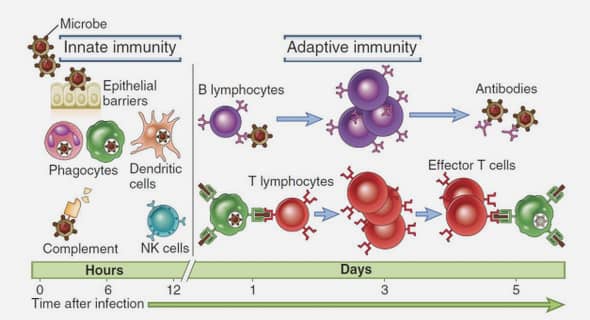
Le pied astrocytaire, constituant de la barrière hémato-encéphalique, est en lien étroit avec la lamina basale de l’endothélium, rendant le domaine extra-cellulaire des canaux AQP4 accessibles aux anticorps. Ceci déclenche ensuite une activation de la voie classique du complément par le C1q aboutissant à des lésions lytiques. Il existe par ailleurs une activation astrocytaire entrainant une réaction inflammatoire via le signalement NF-kB. L’activation du complément engendre une augmentation de la perméabilité de la barrière hémato-encéphalique, aboutissant à un afflux de leucocytes dont les polynucléaires éosinophiles (PNE) et neutrophiles (PNN) qui sont détéctés en grand nombre dans la LCR en phase aigue de la maladie (PNN et PNE > 5/mm3, leucocytes > 50/mm3). Le mécanisme aboutissant à l’apparition de ces anticorps n’est pas entièrement élucidé. Toutefois, il semblerait que dans un premier temps, les peptides de l’AQP4 soient reconnus par les lymphocytes T devenant ainsi des Lymphocytes T Helper 17 qui activeraient à leur tour les lymphocytes B, qui deviendraient des plasmablastes sécrétant des anticorps anti-AQP4 de type IgG1. Ce processus aurait lieu en dehors du SNC.
La physiopathologie des anticorps anti-MOG reste incertaine. Des titres élevés ont été retrouvé dans les populations pédiatriques et moins fréquemment dans les populations adultes atteintes d’encéphalomyélite aigue disséminée (ADEM), de sclérose en plaques (SEP), de NMOSD sans anticorps anti-AQP4 ainsi que dans certains cas isolés de nevrite optique ou de myélite transverse19. La maladie évolue habituellement par des poussées récurrentes. Celles-ci peuvent mettre en jeu le pronostic vital, notamment lors d’atteintes médullaires cervicales étendues. Les patients peuvent garder des séquelles de ces épisodes, notamment motrices, sensitives, optiques et vésico-sphinctériennes, qui en s’accumulant peuvent conduire à un état grabataire4. Une étude sur 71 patients atteints de NMO entre 1950 et 1997 retrouvait dans les formes récurrentes, un taux de mortalité proche d’un tiers, en lien essentiellement avec les poussées de myélite cervicale qui entrainaient des états de détresse respiratoire. Parmi les patients toujours vivants à la fin de l’étude, 60% avaient une acuité visuelle sur au moins un œil < 1/10, et 50% une mono- ou para-plégie4. Ces données sont en partie liées à l’arsenal thérapeutique limité dont nous disposions à l’époque. Une étude multicentrique sur 175 patients entre 2009 et 2011, avec une durée d’observation moyenne de 57.5 mois, rapportait un taux de mortalité de 6% avec une moyenne d’aggravation de l’Expanded Disability Status Scale (EDSS) de 0.65 par an21. La découverte de traitements de poussée ainsi que l’apparition de traitements de fond ont donc changé le pronostic de ces patients.
Traitement de la poussée
Le traitement d’une poussée de NMO repose sur l’utilisation de corticoïdes, en général la Methylprenisolone à posologie de 1 gramme par jour, par voie intra- veineuse, sur 3 à 5 jours en fonction de l’effet et de la tolérance. Un patient ne répondant pas à ce traitement devrait bénéficier de 5 à 7 échanges plasmatiques17,22. Certaines études incitent à utiliser les corticoïdes et les échanges plasmatiques de manière concomittante23. En raison des conséquences potentielles des poussées, la mise en place d’un traitement de fond est nécessaire, quel que soit le statut sérologique du patient24. Contrairement à la SEP, l’utilisation de traitements immunomodulateurs semble inefficace et pourrait même aggraver l’état des patients. Ce sont les immunosuppresseurs qui paraissent les plus efficaces25. Les plus couramment utilisés sont le Rituximab, l’Azathioprine et le Mycophenolate Mofetil22. Une étude comparant ces 3 traitements chez des patients atteints de NMO retrouvait une diminution plus importante du taux annuel de poussées sous Rituximab (de 2.89 à 0.33) et sous Mycophenolate Mofetil (de 2.61 à 0.33) par rapport à l’Azathioprine (de 2.26 à 0.63)26. Une autre étude, montrait une diminution plus importante du taux annuel de poussées chez les patients sous Rituximab (de 1.17 à 0.25) en comparaison à des patients traités par Mycophénolate Mofétil, Azathioprine ou Cyclophosphamide.