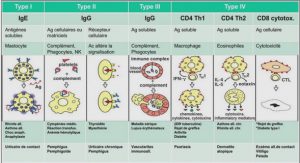
Les principales étapes de l’immunopathologie
Les mécanismes physiopathologiques sont complexes, ils impliquent de nombreux acteurs de l’immunité innée (cytokines, complément, récepteur toll like) et de l’immunité acquise (cellules présentatrices d’antigène, lymphocytes T et B). Ces différents facteurs contribuent au développement d’une inflammation chronique de la membrane synoviale articulaire, la synovite rhumatoïde qui est responsable de la destruction ostéo-cartilagineuse.
Pour rappel, une articulation normale est composée de deux os recouverts de cartilage et délimitée par la capsule articulaire, elle-même tapissée de la membrane synoviale .
La membrane synoviale est impliquée principalement dans la trophicité de l’articulation en sécrétant du liquide synovial qui va lubrifier l’articulation. Les synoviocytes représentent le principal composant cellulaire de la couche bordante (intima) en contact avec la cavité ; ils sont de type fibroblastique principalement, ou de type macrophagique . Les synoviocytes fibroblastiques ont une capacité de prolifération qui ressemble par certains aspects à celle des cellules cancéreuses constituant un panus . La couche sous-intimale (subintima), en contact avec la capsule articulaire, est très vascularisée et comporte des fibroblastes pour moitié .
Enfin, la couche sub-synoviale est riche en mucopolyssaccharides, collagène et cellules adipeuses. Autour de l’articulation, pour la maintenir et la rendre mobile, se trouvent les ligaments et les muscles reliés aux os par les tendons. La synoviale rhumatoïde est caractérisée par une hyperplasie, une hypervascularisation, et un infiltrat cellulaire inflammatoire (essentiellement des lymphocytes T CD4+, lymphocytes B et monocytes-macrophages) qui joue un rôle majeur dans le déclenchement et l’entretien de la réponse immunitaire et inflammatoire . Parallèlement à l’épaississement inflammatoire et prolifératif de la membrane synoviale (synovite), va se constituer le pannus synovial qui est à l’origine de la destruction ostéo-articulaire .
Le rôle des cytokines pro-inflammatoires
Les cytokines pro-inflammatoires jouent un rôle central dans l’inflammation et dans la destruction ostéo-articulaire, qui a été confirmé devant l’efficacité des anti-cytokiniques utilisés dans la PR (anti-TNF-α, anakinra, tocilizumab). Les cytokines sont des glycoprotéines de faible poids moléculaire produites par de très nombreux types cellulaires et qui vont agir, par l’intermédiaire de récepteurs membranaires spécifiques et de signaux de transduction, selon un mode endocrine (action sur les cellules ou tissus distants), paracrine (cellules proches) ou autocrine (sur la cellule productrice ou une cellule proche du même type) . Il s’agit de messagers intercellulaires impliqués dans l’inflammation, la réponse immunitaire et l’hématopoïèse .
Dans la synoviale rhumatoïde, il existe un déséquilibre entre les cytokines à action pro inflammatoire (principalement le TNF-α, l’IL-1, l’IL-6, l’IL-15, IL-17, IL-18) sécrétées en excès principalement par les macrophages, les lymphocytes T et les synoviocytes activés, et les cytokines à action anti-inflammatoire (notamment l’IL-4, l’IL-10, l’IL-13), qui sont présentes en quantité insuffisante. Les cytokines pro-inflammatoires vont agir sur la réaction inflammatoire locale et systémique en induisant la production de protéines de la phase aiguë de l’inflammation (α1 glycoprotéine acide, α1 antichymotrypsine, haptoglobine, C-réactive protéine, sérum amyloïde A protéine etc…) et d’autres médiateurs de l’inflammation (prostaglandine E2, leukotriènes, radicaux libres dont le monoxyde d’azote, chémokines, molécules d’adhésion) . Le TNF-α et l’IL-1 sont capables de stimuler réciproquement leur production et d’induire l’expression d’autres cytokines, comme l’IL-6 , ce qui contribue à l’entretien du processus inflammatoire et immunitaire. A l’inverse, l’IL-6 diminue la production d’IL-1 et de TNF-α.
L’interleukine-6 et la polyarthrite rhumatoïde
L’IL-6 a été isolée au cours de travaux de recherche menés par des équipes étudiant la croissance des plasmocytomes et la production des protéines de la phase aigüe par les hépatocytes. La dénomination d’IL-6 a été adoptée définitivement lors d’une conférence tenue à New York en décembre 1988 .
La Biologie cellulaire : L’IL-6 est une glycoprotéine de 26 kDa constituée de 4 chaînes α et comportant 212 acides aminés . Son gène est situé sur le chromosome 7 humain (7p21) . L’IL-6 est une cytokine pléiotropique produite par un grand nombre de types cellulaires différents, tels que les monocytes/macrophages, les lymphocytes T et B, les mastocytes, les polynucléaires neutrophiles, les éosinophiles, les fibroblastes, les chondrocytes, les adipocytes, les cellules gliales ou encore les cellules endothéliales . Elle exerce ses activités biologiques sur des cibles cellulaires tout aussi variées et impliquées dans de nombreuses pathologies inflammatoires et auto-immunes, dont la PR. L’IL-6 n’est pas exprimée de façon constitutive; sa production nécessite des stimuli inflammatoires tels le lipopolysaccharide (LPS), certaines cytokines ou certains virus (HIV) . Seuls les adipocytes sont capables de produire spontanément l’IL-6 .
Le récepteur à l’IL-6 (CD126 ou gp80) est un hétérodimère constitué d’une chaîne α extra membranaire N- terminal de 80 kDa spécifique de l’IL-6 (IL-6Rs) associé à la gp130, une glycoprotéine transmembranaire ubiquitaire de 130 kDa responsable de la transduction intracellulaire du signal . L’IL-6R existe sous 2 formes, une forme membranaire et une forme soluble. Le récepteur membranaire (IL-6Rm) n’est exprimé de façon constitutive que par certaines cellules (monocytes, macrophages, hépatocytes et certains lymphocytes). Le récepteur soluble (IL-6Rs) est issu du clivage protéolytique de la forme membranaire ou de l’épissage alternatif des ARN messagers codant cette chaîne α . Il est retrouvé dans de nombreux liquides biologiques, notamment dans le liquide synovial et le sérum. La gp 130 (CD130) existe également sous forme soluble (gp130s), cette dernière exerce une activité inhibitrice sur la voie de signalisation de l’IL-6 .
Les traitements médicamenteux actuels de la polyarthrite rhumatoïde
La prise en charge thérapeutique de la PR a connu de véritables bouleversements au cours de ces vingt dernières années. Ces progrès sont liés notamment au développement d’outils médicamenteux plus performants rendu possible grâce à une meilleure connaissance de la physiopathologie de la maladie, ainsi qu’à la démonstration scientifique de nouveaux concepts ayant conduit à de nouvelles stratégies thérapeutiques et à des objectifs plus ambitieux.
Les objectifs thérapeutiques : Une prise en charge thérapeutique précoce est susceptible d’augmenter la probabilité d’obtenir rapidement un état de rémission et de le maintenir, de conduire à une moindre progression structurale, ainsi qu’à une réduction du handicap fonctionnel à long terme . L’un des premiers objectifs sera donc d’obtenir l’avis d’un rhumatologue dans les trois premiers mois afin de confirmer le diagnostic de PR, et d’instaurer dans les plus brefs délais un traitement de fond suffisamment efficace . A court terme, le principal objectif de la prise en charge de la PR est l’obtention d’une rémission (DAS 28 < 2,6) précoce et durable de la maladie, ou tout au moins un faible niveau d’activité (low disease activity) (DAS 28 < 3,2) dans les PR anciennes . Il a été démontré qu’une rémission persistante empêche la progression structurale dans la grande majorité des cas, permettant ainsi de limiter le handicap fonctionnel sur le long terme . A moyen terme, la prévention des érosions et des déformations articulaires constitue un enjeu majeur. L’objectif à plus long terme vise à prévenir le handicap locomoteur et à réduire la mortalité grâce à une attitude préventive vis-à-vis du risque infectieux et du risque cardiovasculaire . Les principales molécules disponibles : Actuellement, la prise en charge médicamenteuse de la PR repose d’une part sur les thérapeutiques à visée symptomatique (les antalgiques, les anti-inflammatoires non stéroïdiens et les corticostéroïdes) permettant de soulager les douleurs et l’inflammation de la PR; et d’autre part sur les traitements dits « de fond » susceptibles de ralentir voire de bloquer l’évolution de la maladie et qui comportent les traitements de fonds conventionnels, aussi connus sous le terme de DMARDS (Disease-Modifying Antirheumatic Drugs), et les biomédicaments.
Etant donné leur délai d’action, les traitements de fond sont généralement associés à un anti inflammatoire à action immédiate (anti-inflammatoires non stéroïdiens, corticoïdes) et/ou à un antalgique, dans le but de soulager rapidement le patient.
Table des matières
INTRODUCTION
PARTIE I : GENERALITES SUR LA POLYARTHRITE RHUMATOIDE
I. La physiopathologie de la polyarthrite rhumatoïde
I-1. Les principales étapes de l’immunopathologie
I-2. Le rôle des cytokines pro-inflammatoires
I-3. L’interleukine-6 et la polyarthrite rhumatoïde
I-3-1. La Biologie cellulaire
I-3-2. Le rôle de l’IL-6 dans la physiopathologie de la polyarthrite rhumatoïde
I-3-2-a. Les effets locaux
I-3-2-b. Les manifestations systémiques
II. Le diagnostic de la polyarthrite rhumatoïde
II-1. La polyarthrite rhumatoïde débutante
II-1-1. Les aspects cliniques
II-1-2. Les aspects biologiques
II-1-2-1. Le syndrome inflammatoire
II-1-2-2. Les auto-anticorps
II-1-2-3. L’examen du liquide synovial
II-1-3. Les aspects à l’imagerie
II-2. La polyarthrite rhumatoïde en phase d’état
II-2-1-1. Les aspects cliniques
II-2-1-2. Les aspects radiographiques
II-2-2. Les manifestations extra-articulaires
III. Les traitements médicamenteux actuels de la polyarthrite rhumatoïde
III-1. Les objectifs thérapeutiques
III-2. Les principales molécules disponibles
III-2-1. Les traitements symptomatiques
III-2-1-1. Les antalgiques
III-2-1-2. Les anti-inflammatoires non stéroïdiens
III-2-1-3. Les glucocorticoïdes
III-2-2. Les traitements de fond
III-2-2-1. Les traitements de fond conventionnels
III-2-2-1-a. Le méthotrexate
III-2-2-1-b. Le léflunomide
III-2-2-1-c. La sulfasalazine
III-2-2-2. Les biomédicaments
III-2-2-2-a. Les anti-TNF-α
III-2-2-2-b. L’anakinra
III-2-2-2-c. Le rituximab
III-2-2-2-d. L’abatacept
III-3. Les stratégies thérapeutiques
IV. Le tocilizumab
IV-1. Les caractéristiques du produit
IV-1-1. Modalités de prescription et de délivrance
IV-1-2. Formes pharmaceutiques
IV-1-3. Structure moléculaire et mécanisme d’action
IV-1-4. Indications et place dans la stratégie thérapeutique de la polyarthrite rhumatoïde
IV-1-5. Posologie et mode d’administration
IV-1-6. Pharmacocinétique
IV-1-7. Tolérance et effets indésirables
IV-1-8. Interactions médicamenteuses
IV-1-9. Grossesse et allaitement
IV-1-10. Bilan pré-thérapeutique
IV-1-11. Suivi thérapeutique
IV-2. Les principaux essais cliniques sur le TCZ au cours de la polyarthrite rhumatoïde
IV-2-1. Les principaux critères de jugement
IV-2-2. L’efficacité du tocilizumab
IV-2-3. Conclusion
PARTIE II : IDENTIFICATION DE FACTEURS PREDICTIFS DE REPONSE ET DONNEES DE TOLERANCE
I. Objectifs
II. Patients & méthodes
II-1. Patients
II-2. Méthodes
II-2-1. Données démographiques
II-2-2. Données cliniques
II-2-3. Données biologiques
II-2-4. Evaluation de l’efficacité
II-2-5. Evaluation de la tolérance
II-2-6. Tests statistiques
III. Résultats
III-1. Description de la population étudiée
III-1-1. Données démographiques
III-1-2. Traitements associés (DMARDs, corticothérapie)
III-1-3. Traitements de fond antérieurs (DMARDs, biomédicaments)
III-2. Réponse clinique et biologique au tocilizumab
III-2-1. Evaluation clinique et biologique avant la première perfusion (J0)
III-2-2. Evaluation de la réponse clinique et biologique après 1, 3 et 6 mois de traitement
III-3. Recherche de facteurs prédictifs de réponse au TCZ à 6 mois de traitement
III-3-1. Comparaison des variables à J0 entre les patients en rémission à M6 versus les
autres patients
III-3-2. Comparaison des variables à J0 entre les patients bons répondeurs EULAR à M6 versus les autres patients
III-3-3. Comparaison des variables à J0 entre les patients en rémission ou en LAD à M6 versus les autres patients
III-4. Tolérance
IV. DISCUSSION
CONCLUSION
ANNEXE
BIBLIOGRAPHIE