CLASSIFICATION, STRUCTURE CHIMIQUE ET PROPRIETES DES PRINCIPAUX ANTIPALUDEENS
Depuis le début du 20è siècle, des milliers de molécules ont été sélectionnées pour leurs activités antipaludiques, mais seules quelques-unes se sont avérées efficaces et ont été utilisées. Jusqu’à présent, les efforts pour produire un vaccin efficace contre le paludisme ont été vains.8 D’où la nécessité de développer de nouveaux médicaments antipaludiques. Les médicaments antipaludiques peuvent être classés selon plusieurs critères : selon leur origine et la nature de leur structure chimique.
Classification des médicaments antipaludiques
Antipaludéens naturels : la Quinine (QN) (Quinquina) et les autres alcaloïdes du quinquina, et l’Artémisinine (ART) (Artémisia annua L.). Antipaludéens synthétiques : tous les autres médicaments antipaludiques. I.2. Classification chimique : Les dérivés quinoléiques : dans ce groupe on retrouve les 4-aminoquinoléines : Chloroquine, Amodiaquine ; les aminoalcools quinoléiques ou arylméthanols : Quinine et ses dérivés alcaloïdes ; Méfloquine, Amodiaquine et les 8- aminoquinoléines : Pamaquine, Primaquine, etc. Les dérivés antracéniques ou aminoalcools antracéniques : dans ce groupe on retrouve : l’Halofantrine et la Luméfantrine (Benfluméthol), un dérivé apparenté mais non antracénique. Lafran®,etc…) La Quinine est à la fois le plus ancien et le plus précieux des antipaludéens pour le traitement du paludisme grave par voie de perfusion intraveineuse (IP) ou par voie rectale (IR) chez l’enfant.9 Elle a été isolée pour la première fois en 1820 par P. J. Pelletier et J. Caventou des écorces de quinquina (Cinchona spp) dont les vertus thérapeutiques ont été découvertes en 1630 au Pérou.
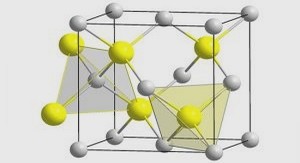
Le quinquina pousse de manière spontanée au Pérou et en Bolivie. Mais elle est cultivée dans les plaines de Java, en Indonésie, en Inde et en Afrique centrale. Ces trois dernières régions sont d’ailleurs les principales régions productrices de Quinine. La structure moléculaire de la Quinine a pour la première fois été décrite en 1907 par P. Rabe et al.10 Elle est formée de deux noyaux quinoléine et quinuclidine, lesquels sont reliés Des études de relation structure-activité réalisées sur la molécule de Quinine ont montré que le groupe OH est indispensable à l’activité antipaludique. En effet son remplacement par un halogène donne lieu à des composés inactifs. La saturation du groupe vinyle ne change pas cependant l’activité. En revanche, son oxydation en COOH annihile première synthèse totale a été réalisée en 1944 par Woodward et Doering.14, 15 Un nouveau procédé de synthèse totale a été décrit en 2004 par Raheem et al.16 La première synthèse totale stéréosélective de la Quinine a été réalisée par Stork et al en 2001.17 Les procédés de synthèse totale de la Quinine sont cependant trop complexes et comportent beaucoup d’étapes pour être commercialement rentables. Ainsi, la Quinine continue d’être isolée par voie d’extraction chimique.
La Quinidine
En dehors de ses propriétés antipaludiques, la Quinine a aussi des propriétés catalytiques. Elle intervient dans de nombreuses réactions de synthèse asymétrique. Elle possède en effet 4 stéréocentres : C3, C4, C8 et C9. Ainsi, elle se présente sous la forme configurationnelle (-)-8R, 9S. Elle est diastéréoisomère à la Quinidine (+)-8R, 9S. Elle a été isolée une douzaine d’années après la découverte de la Quinine et de la Cinchonine. Elle est une modification isomérique de la Quinine. Mais les deux sont images optiques l’une de l’autre au niveau des atomes de carbone C8 et C9. La Cinchonine (-)-8S, 9R : isolée à l’état impur par Duncan en 1803, elle a été obtenue pour la première fois à l’état de pureté et cristallisée par le Docteur Gomez de Lisbonne en 1810. C’est en 1820 que Pelletier et Caventou l’ont obtenu à l’état pur de eaux mères de l’extraction de la Quinine. Médicament antipaludique souvent prescrit dans les cas de paludisme grave, le Quinimax® est ainsi une combinaison archaïque de la Quinine, la que l’activité décroît dans le sens: Quinidine > Quinine > Cinchonine > Cinchonidine. Les 4 stéréoisomères de configuration Erythro sont actifs, alors que leur diastéréoisomère de Dans ce groupe, on retrouve l’Artémisinine ou Quinghaosu et ses dérivés de première génération: la Dihydroartémisinine, l’Artéméther, l’Artéether et l’Artésunate.
Ils sont structuralement proches de la Quinine. Les médicaments 4-AQ agissent dans la plupart du temps au cours des stades sanguins du cycle de vie du parasite30 mais certains sont également soupçonnés de cibler le stade hépatique.31 Dans ce groupe, on retrouve la Par la suite sa structure a été modifiée par l’adjonction d’une chaine dialkylaminoalkane. La molécule obtenue à cet effet s’est révélée plus active que le BM parent lui-même. La modification chimique du chromophore du BM a servi ensuite à la mise au point des 8-aminoquinoléines et des 4-aminoquinoléines.33, 34 Actuellement le BM est en développement clinique en combinaison avec l’Amodiaquine (voir schéma 25). est constituée d’un noyau quinoléique qui, lui-même, est substitué en position 7 par un atome de chlore et en position 4 par une chaîne diaminobutane. Elle porte aussi le groupe méthyle sur la chaîne alcoylée, ce qui a donné lieu à un centre stéréogénique.