Biomarqueur salivaire d’exposition de l’homme aux
piqûres des vecteurs du paludisme
Protéines salivaires synthétiques comme marqueurs immunologiques d’exposition
Le développement d’un test biologique mesurant l’exposition de l’hôte aux piqûres d’arthropodes hématophages se heurte à des difficultés majeures que sont le recueil de la salive ou des extraits de glandes salivaires et le manque de standardisation de l’échantillonnage. En effet, la teneur et la composition en protéines salivaires d’arthropodes hématophages peuvent varier en fonction du sexe, de l’âge ou du régime alimentaire (Volf et al. 2000 ; Prates et al. 2008). Ainsi, l’identification des protéines salivaires immunogéniques Implication de la salive des arthropodes hématophages dans les relations hôtevecteur et ses applications 75 spécifiques au genre ou à l’espèce et leur production sous forme recombinante ou de peptides synthétiques (Tableau 2) permettrait d’obtenir un gain de sensibilité, de spécificité et de reproductibilité dans les tests immunologiques. Figure 17 : Les séquences des protéines gSG6 d’Anopheles (Lombardo et al. 2009). (A) Alignement des séquences de gSG6 de 8 espèces d’Anopheles. Les peptides signaux et les cystéines conservées sont encadrés. Les sites conservés sont grisés. (B) Arbre phylogénétique construit à partir de l’alignement de la séquence nucléotidique codant pour les polypeptides matures de gSG6. La protéine recombinante gSG6 d’An. gambiae (An. gambiae Salivary Gland protein 6), une petite protéine hautement conservée dans le genre Anopheles (Lombardo et al. 2009), a été évaluée comme un marqueur immunologique d’exposition (Poinsignon et al. 2008b). La protéine recombinante gSG6 a été détectée par les anticorps IgG des enfants exposés aux piqûres d’An. gambiae. L’analyse BLAST, Basic Local Alignment Search Tool (NCBInr, NIH, Bethesda, 15 Novembre 2010), a révélé que les protéines homologues de la gSG6 se Implication de la salive des arthropodes hématophages dans les relations hôtevecteur et ses applications 76 retrouvent chez 8 autres espèces d’Anopheles (Lombardo et al. 2009) (Figure 17), suggérant sa spécificité au genre Anopheles. Cette protéine a récemment été proposée comme un candidat marqueur sérologique d’exposition aux vecteurs du paludisme Afro-tropical (Rizzo et al. 2011). Les individus exposés aux tiques Amblyomma americanum et Dermacentor variabilis développement également une réponse IgG spécifique contre la protéine calréticuline recombinante (rTC, recombinant Tick Calreticulin) isolée à partir des glandes salivaires de tiques A. americanum (Sanders et al. 1998). L’utilisation des protéines salivaires recombinantes hautement conservées entre plusieurs espèces vectrices apparentées pourrait être utile dans l’évaluation du risque de transmission chez les individus vivant dans des zones où la diversité des espèces vectrices n’est pas bien caractérisée ou même applicable dans des zones qui présentent des espèces vectrices différentes. Fait intéressant, la séropositivité des anticorps anti-rTC a une plus grande spécificité (mais une sensibilité plus faible) que les anticorps dirigés contre la salive totale pour détecter les individus qui ont été exposés aux piqûres de tique (Sanders et al. 1999). Ce manque de sensibilité pourrait être expliqué par l’utilisation d’une seule protéine salivaire recombinante pour évaluer l’exposition individuelle aux piqûres de tiques. En effet, il a été rapporté, dans le cas de la leishmaniose, que l’utilisation de deux protéines salivaires recombinantes (nommées LJM17 et LJM11) était plus efficace et plus sensible que l’utilisation de la salive totale pour estimer le niveau d’exposition à Lutzomia longipalpis (Teixeira et al. 2010 ; Souza et al. 2010). Les protéines recombinantes, produites principalement pour leurs propriétés biologiques ou leur rôle dans les réactions allergiques (Tableau 2), pourraient également être considérées comme de potentiels candidats marqueurs d’exposition. Certaines de ces protéines semblent être relativement spécifiques à une famille ou un genre de vecteur et pourraient être des marqueurs épidémiologiques prometteurs d’exposition aux vecteurs. Ribeiro et al. (2010) ont classé les protéines salivaires conservées à différents niveaux taxonomiques, dans le sousordre des Nématocera à partir duquel d’autres candidats antigènes spécifiques pourraient émerger. La détection et la sélection de peptides spécifiques dans la séquence des protéines salivaires pourraient encore accroitre la spécificité de ces marqueurs immunologiques et réduire les coûts liés à la production. Afin d’optimiser la spécificité du marqueur gSG6, une stratégie « peptide » a été développée par Poinsignon et al. (2008b) en combinant des analyses Implication de la salive des arthropodes hématophages dans les relations hôtevecteur et ses applications 77 bioinformatiques et des alignements de séquences. Elle consiste en i) une identification des épitopes immunogènes potentiels prédits par des algorithmes disponibles en ligne sur internet, et ii) une vérification de sa spécificité à Anopheles par des comparaison de séquences (programme BLAST) des principaux vecteurs (base de données VectorBase) mais aussi de tous les organismes via la base de données GenBank. Cette stratégie a permis d’aboutir à l’identification de 5 peptides antigéniques (gSG6-P1 à gSG6-P5). Cependant, le gSG6-P1 semblait être le plus pertinent comme candidat marqueur d’exposition. En effet, une association positive entre la réponse IgG anti-gSG6-P1 et le niveau d’exposition, a été observée chez les individus exposés aux piqûres d’An. gambiae (Poinsignon et al. 2008b). Une réponse IgG dirigée contre le gSG6-P1 a également été détectée chez des personnes exposées à un très faible nombre de piqûres d’An. gambiae (Poinsignon et al. 2009), ce qui suggère son potentiel à détecter une exposition à An. gambiae dans un contexte de faible exposition, contexte dans lequel les méthodes entomologiques classiques présentent des limites de sensibilité (zones urbaines, altitude, saison sèche…). En outre, des études ont montré que la séquence gSG6-P1 (Figure 18) est très conservée entre espèces d’Anopheles (Calvo et al. 2007 ; Lombardo et al. 2009). Cela indique que ce peptide peut être un biomarqueur potentiel aux autres espèces d’anophèles vecteurs. A ce sujet, une étude effectuée au Sénégal a montré que la réponse IgG anti-gSG6-P1 constitue également un biomarqueur d’exposition à An. funestus (Poinsignon et al. 2010). Figure 18 : Alignements des séquences de gSG6 chez 3 espèces d’Anopheles, An. stephensi (AS), An. funestus (AF) et An. gambiae (AG) (Calvo et al. 2007). L’encadré en rouge indique la séquence gSG6-P1 de ces trois anophèles vecteurs. Récemment, l’utilisation du biomarqueur salivaire d’exposition aux piqûres d’anophèles (réponse IgG anti-gSG6-P1) a permis d’évaluer le risque de transmission du paludisme chez des enfants et des adultes vivant dans une zone urbaine du Sénégal (région de Dakar) (Drame Implication de la salive des arthropodes hématophages dans les relations hôtevecteur et ses applications 78 et al. 2012). En effet, une variation considérable des taux d’IgG anti-gSG6-P1 a été observée chez les individus vivants au sein du même district et entre des districts différents, et ceci en dépit du niveau d’exposition globalement faible (données entomologiques). Ce biomarqueur semble donc être un outil pertinent pour évaluer l’hétérogénéité d’exposition au risque de paludisme urbain. Le développement d’un tel outil serait particulièrement pertinent pour la cartographie et la surveillance du risque de paludisme, mais également pour l’évaluation de l’efficacité des stratégies de lutte anti-vectorielle mises en œuvre dans ces zones particulières.
Zone et population d’étude
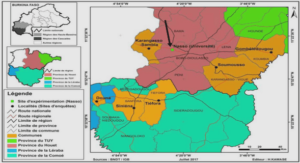
Notre étude a été menée dans la région Nord du Sénégal, au niveau du district de Podor, en bordure du Fleuve Sénégal qui marque la frontière avec la Mauritanie (Figure 19). Dans cette partie du pays, le climat est de type sahélien avec une longue saison sèche de novembre à juin faisant suite à une courte saison pluvieuse (dite hivernage) de juillet à octobre (précipitation annuelle <400 mm). La moyenne de température oscille entre 25 et 30°C durant la saison fraîche (novembre à février) et 25 à 40°C durant la saison chaude (mars à octobre). La végétation est éparse avec très peu d’arbres à l’intérieur et autour des villages. Dans cette zone, les activités principales sont l’agriculture (mil, riz, maïs, arachide, haricot, niébé, maraîchage) et l’élevage de zébus et petits ruminants. Du fait de la proximité du fleuve Sénégal et de la présence d’infrastructures hydrauliques (barrages, canaux, bassins de rétention), l’irrigation est couramment pratiquée et permet un calendrier cultural s’étendant tout au long de l’année. L’habitat traditionnel est fait de murs en banco avec un toit de chaume sur une armature en bois. Mais on rencontre aussi des maisons modernes en bloc de ciment et toit en tôle ondulée. La zone est considérée comme hypo-endémique à méso-endémique pour le paludisme à P. falciparum (moins de 10 ou entre 10 et 100 piqûres infectantes par homme et par an, respectivement) (Dia et al. 2008 ; Ndiath et al. 2012). Comme conséquence de la faible transmission, la morbidité due au paludisme y est très faible (<5 cas de paludisme pour 1000 habitants) (PNLP 2010). La transmission du paludisme est principalement assurée par les anophèles appartenant au complexe An. gambiae (Ndiath et al. 2012) et a lieu au cours de la saison des pluies et quelques mois après. Les sites pouvant servir de gîtes larvaires sont nombreux dans la zone : bords du fleuve Sénégal et ses ramifications, canaux d’irrigation, mares temporaires… Les autres pathologies infantiles couramment rencontrées dans la zone sont les infections pulmonaires, les entérites aigues, la bilharziose… La malnutrition chronique y est estimée à 15% pour les enfants de moins de 5 ans (Gaayeb et al. 2014). Plusieurs ethnies sont rencontrées au sein de la population dans la zone d’étude : Peuls, Wolofs, Maures. Dans les villages inclus dans notre étude, les Peuls sont généralement majoritaires.
Choix et description des villages
Le choix des 5 villages d’étude (Agnam Tonguel, Guédé Village, Niandane, Pendao et Fanaye Diéry) a été effectué, suite a une étude entomologique prospective menée dans 20 villages de la zone en septembre 2008 par des membres de l’Unité de Recherche sur les Maladies Infectieuses et Tropicales Emergentes (URMITE) de l’IRD (Institut de Recherche pour le Développement) de Dakar. Le principal critère d’inclusion de ces villages est la présence d’An. gambiae s.l. comme vecteur majeur et leur niveau d’exposition. En plus du facteur entomologique, d’autres critères ont été pris en compte pour le choix des villages : le nombre d’habitants qui devait permettre de recruter un nombre suffisant d’enfants pour l’étude, une couverture vaccinale suffisante (>70%), l’accessibilité du village, la présence d’ICP (Infirmier Chef de Poste) ou d’ASC (Agent de Santé Communautaire) pour facilité le suivi médical des enfants et bien entendu l’accord des autorités locales de chaque village. Tous ces villages se situent à moins d’un kilomètre de bras du fleuve Sénégal.
Les villages de Agnam Tonguel et de Guédé Village
Les villages de Agnam Tonguel (16°32’ N-14°48’ W) et de Guédé Village (16°33’ N-14°48) sont situés de part et d’autre du fleuve Doué, à 50 km de Podor. Outre la lame d’eau du Doué, le réseau hydrographique est principalement constitué de mares temporaires qui se remplissent pendant hivernage et s’assèchent en saison sèche. En 2000, Agnam Tonguel et Description de l’étude de cohorte 83 Guédé Village étaient peuplés, respectivement, d’environ 684 et 1633 habitants avec, essentiellement, des Peuls comme ethnie majoritaire. Le maraîchage reste la principale activité agricole pendant la saison sèche. Le cheptel est essentiellement constitué d’ongulés qui passent la nuit dans le village à proximité des habitations. Les habitations sont principalement de types traditionnels, mais on note également la présence de quelques habitations modernes.
Le village de Niandane
Le village de Niandane (16°35’ N-14°59’ W) est situé à une trentaine de kilomètres au Sud de Podor. En 2000, la population comptait environ 4815 habitants appartenant, en majorité, à l’ethnie Wolof. Les habitations sont surtout de types modernes, mais on note également la présence de quelques habitations traditionnelles. Le réseau hydrographique est représenté, d’une part, par le fleuve Sénégal et le Doué et, d’autre part, par les canaux d’irrigation instaurés par la SAED (Société Nationale d’Aménagement et d’Exploitation des Terres du Delta du fleuve Sénégal et des Vallées du fleuve Sénégal et de la Falémé), pour la riziculture irriguée. L’agriculture demeure la principale activité dans ce village. Le mil, le niébé et les pastèques sont les principales spéculations cultivées pendant la saison des pluies, tandis que le maraîchage (oignons) reste la principale activité agricole pendant la saison sèche. L’élevage est peu développé et le bétail (chèvres, moutons et bœufs) est emmené pendant le jour en pâturage et ramené la nuit où il est parqué dans des enclos à l’intérieur des concessions.
Les villages de Pendao et de Fanaye Diéry
Les villages de Pendao (16°30 N-15°03’ W) et de Fanaye Diéry (16°32’N-15°13’ W) sont situés au Sud-Est de Podor, entre le fleuve Ngalanka et la route nationale n°2, à l’entrée du Fouta. En 2000, la population était estimée à 2207 habitants et 6875 habitants, respectivement à Pendao et à Fanaye Diéry. Cette population est composée essentiellement de Peuls, Wolofs et Maures. Les habitations sont de types variés (traditionnels et modernes). Les habitations traditionnelles sont surtout transformées en greniers et sont progressivement remplacées par des habitations modernes. La source d’eau permanente la plus proche est représentée par le fleuve Ngalanka et des bassins de rétention servant à irriguer les périmètres agricoles aménagés à proximité des villages. Cet aménagement permet aux villageois de pratiquer deux cycles de culture de riz et un maraîchage permanent. L’élevage est très développé et le cheptel est essentiellement constitué de bovins, ovins et caprins, avec une végétation abondante. Description de l’étude de cohorte
Recrutement de la cohorte
La cohorte est constituée de 410 enfants âgés de 1 à 9 ans et répartis comme suit dans les 5 villages : 48 enfants à Guédé Village, 53 enfants à Agnam Tonguel, 101 enfants à Pendao, 103 enfants à Niandane et 105 enfants à Fanaye Diéry. Le faible nombre d’enfants recrutés à Guédé Village et à Agnam Tonguel est dû au fait que ces deux villages, séparés uniquement par un bras du fleuve Sénégal, devaient initialement être traités comme un seul village en raison de leur proximité et du poste de santé qui leur est commun. Mais, ils ont finalement été traités séparément en raison d’un niveau d’exposition aux anophèles différent que nous avons noté au cours de nos travaux. L’étude a été approuvée par le Comité National de Recherche en Santé (CNRS) du Sénégal en octobre 2008 (0084/MSP/DS/CNRS, clinicaltrials.gov/ct2/show/NCT01545115) et le consentement éclairé a été obtenu de la part des parents ou des tuteurs des enfants. En contrepartie de la participation des enfants, les médicaments adaptés aux pathologies rencontrées couramment étaient fournis aux postes de santé et délivrés gratuitement par les infirmiers en cas de nécessité.
Dédicaces |